Resúmenes de los trabajos académicos de nuestros becados
2015/5/12
Estudio sobre las dependencias intrínsecas de las actividades fotocatalíticas sobre las propiedades estructurales y físicas de fotocatalizadores de óxido de titanio (IV)
Orlando Omar Prieto Mahaney
Universidad de Hokkaido
2009
Universidad de Hokkaido
2009
Introducción
El área en la que estoy actualmente trabajando, y en la que hice mi tesis doctoral, es en realidad un área multidisciplinaria que requiere de la Ciencia de los Materiales, Catálisis, Fisicoquímica y Ciencia Medioambiental para cumplir sus objetivos. Eso permite utilizar el conocimiento obtenido para, por ejemplo, la preparación de nuevos materiales con aplicaciones en la generación de fuentes de energía alternativa o en el cuidado del medio ambiente. Mi tesis doctoral trata acerca de uno de esos materiales, el dióxido de titanio, que puede ser utilizado en una infinidad de campos. Los más prometedores son el de generación de energía alternativa y su capacidad como agente de limpieza de contaminantes ambientales. Pero, para poder utilizar dióxido de titanio es necesario primero conocerlo con detalle.
El dióxido de titanio (o simplemente 'titania') es un material compuesto de titanio y oxígeno, TiO2, que es clasificado como 'semiconductor' porque a diferencia de los metales (o conductores) sólo es capaz de conducir electricidad bajo determinadas circunstancias, las cuales están determinadas por su característica estructura íntima. Como toda sustancia química las titanias están compuestas de átomos en un arreglo ordenado (estructura cristalina) que les confiere una estructura electrónica particular y única. La 'teoría de bandas' (que considera a los electrones acomodados en bandas) fue originalmente usada para describir a los metales, pero sirve muy bien para describir también a los semiconductores como la titania.
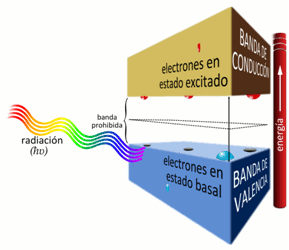
La imagen muestra esquemáticamente cómo los electrones están acomodados dentro de un semiconductor, en este caso titania. La mayoría están en su estado basal (o fundamental) y consumen poca energía formando la 'banda de valencia' (BV). Si energía (radiación) con la capacidad suficiente alcanza a estos electrones en la BV, estos son capaces de ser transferidos a niveles de energía superiores formando la 'banda de conducción' (BC). Sin la energía necesaria los electrones permanecen en estado basal separados de la BC por un espacio conocido como 'banda prohibida'. Los electrones que son transferidos (proceso conocido como transición electrónica) a la BC dejan espacios vacíos en la BV, o 'huecos'. Ya que los electrones son negativos, la BC será negativa, y la BV, debido a esos espacios vacíos, será positiva. A estos pares de electrones (e-) y huecos positivos (h+) se denomina 'pares e-/h+', y son altamente reactivos y responsables de procesos químicos conocidos como 'redox' (REDucción y OXidación).
El dióxido de titanio (o simplemente 'titania') es un material compuesto de titanio y oxígeno, TiO2, que es clasificado como 'semiconductor' porque a diferencia de los metales (o conductores) sólo es capaz de conducir electricidad bajo determinadas circunstancias, las cuales están determinadas por su característica estructura íntima. Como toda sustancia química las titanias están compuestas de átomos en un arreglo ordenado (estructura cristalina) que les confiere una estructura electrónica particular y única. La 'teoría de bandas' (que considera a los electrones acomodados en bandas) fue originalmente usada para describir a los metales, pero sirve muy bien para describir también a los semiconductores como la titania.
La imagen muestra esquemáticamente cómo los electrones están acomodados dentro de un semiconductor, en este caso titania. La mayoría están en su estado basal (o fundamental) y consumen poca energía formando la 'banda de valencia' (BV). Si energía (radiación) con la capacidad suficiente alcanza a estos electrones en la BV, estos son capaces de ser transferidos a niveles de energía superiores formando la 'banda de conducción' (BC). Sin la energía necesaria los electrones permanecen en estado basal separados de la BC por un espacio conocido como 'banda prohibida'. Los electrones que son transferidos (proceso conocido como transición electrónica) a la BC dejan espacios vacíos en la BV, o 'huecos'. Ya que los electrones son negativos, la BC será negativa, y la BV, debido a esos espacios vacíos, será positiva. A estos pares de electrones (e-) y huecos positivos (h+) se denomina 'pares e-/h+', y son altamente reactivos y responsables de procesos químicos conocidos como 'redox' (REDucción y OXidación).
Primera parte

En la primera parte de mi tesis he trabajado con 5 reacciones químicas diferentes, para probar la capacidad fotocatalítica de 40 diferentes muestras comerciales de titania. Es decir, utilizando luz (radiación) se puede estudiar la capacidad de la titania para reducir materiales contaminantes (metanol, acetaldehído), generar fuentes alternativas de combustible (oxígeno, hidrógeno) o para sintetizar materiales de interés médico utilizando medios alternativos de preparación (síntesis de ácido pipecolínico). Además se estudió las propiedades físicas y químicas de estos 40 fotocatalizadores (denominados así por su capacidad de reaccionar con radiación sin modificar su naturaleza), como tamaño de partícula, composición química, área de superficie específica, número de defectos, etc. Toda esta cantidad de datos fue agrupada y analizada utilizando métodos matemáticos (matrices y estadística) para determinar la relación entre la actividad fotocatalítica (o velocidad de reacción) y las propiedades de cada sustancia.
Los resultados de ese análisis demostraron, por primera vez, que sí es posible describir la velocidad de una reacción química utilizando las propiedades particulares de cada sustancia.
La matriz que se ve en la parte inferior derecha de la Figura 2, representa a los 'coeficientes' que expresan el grado en que cada propiedad física (seis propiedades, seis coeficientes) contribuye a la velocidad de reacción. Es evidente que mientras más propiedades se tengan mejor se expresará la valocidad de reacción. El problema está en escoger las propiedades adecuadas, ¿cómo hacerlo? La parte tercera de mi tesis trata de ese punto particular. Pero antes, vamos a la segunda parte, el estudio de un fotocatalizador particular.
Los resultados de ese análisis demostraron, por primera vez, que sí es posible describir la velocidad de una reacción química utilizando las propiedades particulares de cada sustancia.
La matriz que se ve en la parte inferior derecha de la Figura 2, representa a los 'coeficientes' que expresan el grado en que cada propiedad física (seis propiedades, seis coeficientes) contribuye a la velocidad de reacción. Es evidente que mientras más propiedades se tengan mejor se expresará la valocidad de reacción. El problema está en escoger las propiedades adecuadas, ¿cómo hacerlo? La parte tercera de mi tesis trata de ese punto particular. Pero antes, vamos a la segunda parte, el estudio de un fotocatalizador particular.
Segunda parte
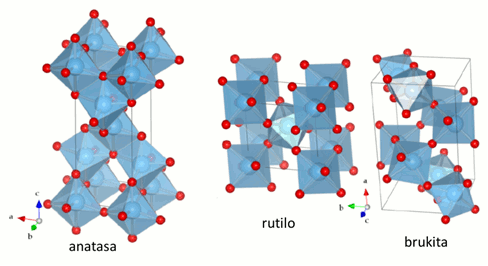
Uno de los fotocatalizadores basados en titania más conocido es denominado Degussa P25 (o sólo P25). Esta sustancia es considerada como modelo de fotocatalizador y, en muchos casos, como material de referencia aún a pesar de que su verdadera composición no está completamente descrita. La proporción y estructura del P25 no había sido clarificada hasta esta tesis y sólo se la mencionaba como una mezcla compuesta por dos de sus formas cristalinas conocidas, anatasa y rutilo, teniendo aproximadamente 80 y 20 por ciento cada una en el fotocatalizador P25. La apariencia de cada fase (estructura cristalina) puede verse en la figura de abajo.
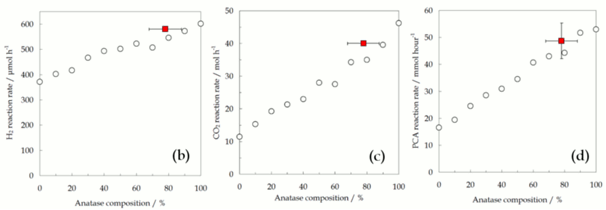
En mi tesis de grado se pudo determinar la composición precisa de una muestra dada de P25 utillizando un método de disolución para cada fase que permitió la separación de las fases aisladas de anatasa y rutilo a partir de P25. Cada fase se analizó utilizando métodos de difracción de rayos X y, por medio de un indicador sólido interno, óxido de níquel, y utilizando diferentes mezclas de las fases separadas, se pudo construir curvas de calibración para cada fase cristalina lo que permitió determinar, por primera vez, la composición cristalina de una muestra cualquiera de P25, incluyendo su fase amorfa. Adicionalmente, a partir de estos resultados, se estudiaron las mismas reacciones químicas que se mencionan en la primera parte de esta tesis, pero utilizando las mezclas (en diferentes proporciones) de anatasa y rutilo. Los resultados sugieren que la misteriosa sinergia atribuída a P25 es inexistente y que este fotocatalizador parecer ser simplemente una mezcla cuyas fases cristalinas trabajan independientemete la una de la otra.
En mi tesis de grado se pudo determinar la composición precisa de una muestra dada de P25 utillizando un método de disolución para cada fase que permitió la separación de las fases aisladas de anatasa y rutilo a partir de P25. Cada fase se analizó utilizando métodos de difracción de rayos X y, por medio de un indicador sólido interno, óxido de níquel, y utilizando diferentes mezclas de las fases separadas, se pudo construir curvas de calibración para cada fase cristalina lo que permitió determinar, por primera vez, la composición cristalina de una muestra cualquiera de P25, incluyendo su fase amorfa. Adicionalmente, a partir de estos resultados, se estudiaron las mismas reacciones químicas que se mencionan en la primera parte de esta tesis, pero utilizando las mezclas (en diferentes proporciones) de anatasa y rutilo. Los resultados sugieren que la misteriosa sinergia atribuída a P25 es inexistente y que este fotocatalizador parecer ser simplemente una mezcla cuyas fases cristalinas trabajan independientemete la una de la otra.
Tercera parte

Finalmente, la tercera parte de mi tesis explora las posibilidades de expandir los resultados encontrados en la primera parte del trabajo. ¿Cuáles propiedas físicas y/o químicas deben ser incluídas como importantes para el análisis de la actividad fotocatalítica en fotocatalizadores de titania? ¿Cómo se pueden seleccionar nuevas propiedas y cómo se las puede incluir en un análisis numérico/estadístico?
Como ejemplo, se incluye a la forma cristalina de la titania, obtenida utilizando dos métodos de síntesis diferentes (hidrólisis y condensación en medio orgánico, y calentamiento y rápido enfriamiento en fase gaseosa) para la preparación de partículas monodispersas ricas en anatasa. Las dos formas cristalinas preparadas fueron estudiadas de la misma manera en lo que fueron las muestras comerciales y aquellas preparadas en la segunda parte de esta tesis. Los resultados mostraron que en muchos casos la actividad fotocatalítica mostrada por estas formas cristalinas de titania eran o similares o superiores que aquellas mostradas por P25. Aunque estos resultados resultaron relativamente prometedores, todavía hay mucho que esclarecer con respecto a los mecanismos que inducen la elevada actividad que presentan estas formas alotrópicas de la titania y el papel que los planos geométricos que cada una presenta frente a potenciales sustancias que sean adsorbidas en sus superficies.
Como ejemplo, se incluye a la forma cristalina de la titania, obtenida utilizando dos métodos de síntesis diferentes (hidrólisis y condensación en medio orgánico, y calentamiento y rápido enfriamiento en fase gaseosa) para la preparación de partículas monodispersas ricas en anatasa. Las dos formas cristalinas preparadas fueron estudiadas de la misma manera en lo que fueron las muestras comerciales y aquellas preparadas en la segunda parte de esta tesis. Los resultados mostraron que en muchos casos la actividad fotocatalítica mostrada por estas formas cristalinas de titania eran o similares o superiores que aquellas mostradas por P25. Aunque estos resultados resultaron relativamente prometedores, todavía hay mucho que esclarecer con respecto a los mecanismos que inducen la elevada actividad que presentan estas formas alotrópicas de la titania y el papel que los planos geométricos que cada una presenta frente a potenciales sustancias que sean adsorbidas en sus superficies.
